АТФ в биологии – определение и расшифровка (10 класс)
В биологии АТФ – это источник энергии и основа жизни. АТФ – аденозинтрифосфат – участвует в процессах метаболизма и регулирует биохимические реакции в организме.

Что это?
Понять, что такое АТФ, поможет химия. Химическая формула молекулы АТФ – C10h26N5O13P3. Запомнить полное название несложно, если разбить его на составные части. Аденозинтрифосфат или аденозинтрифосфорная кислота – нуклеотид, состоящий из трёх частей:
- аденина – пуринового азотистого основания;
- рибозы – моносахарида, относящегося к пентозам;
- трёх остатков фосфорной кислоты.
Рис. 1. Строение молекулы АТФ.
Более подробная расшифровка АТФ представлена в таблице.
Составные части | Формула | |
Аденин | C5H5N5 | Производное пурина, входит в состав жизненно важных нуклеотидов. Не растворим в воде |
Рибоза | C5h20O5 | Пятиуглеродный сахар, входящий в состав нуклеотидов, в том числе РНК |
Фосфорная кислота | Н3РО4 | Неорганическая кислота, быстро растворимая в воде |
АТФ впервые обнаружили гарвардские биохимики Суббарао, Ломан, Фиске в 1929 году. В 1941 году немецкий биохимик Фриц Липман установил, что АТФ является источником энергии живого организма.
Образование энергии
Фосфатные группы соединены между собой высокоэнергетическими связями, которые легко разрушаются. При гидролизе (взаимодействии с водой) связи фосфатной группы распадаются, высвобождая большое количество энергии, а АТФ превращается в АДФ (аденозиндифосфорную кислоту).
Условно химическая реакция выглядит следующим образом: ТОП-4 статьикоторые читают вместе с этойАТФ + Н2О → АДФ + Н3РО4 + энергия
Рис. 2. Гидролиз АТФ.
Часть высвободившейся энергии (около 40 кДж/моль) участвует в анаболизме (ассимиляции, пластическом обмене), часть – рассеивается в виде тепла для поддержания температуры тела. При дальнейшем гидролизе АДФ отщепляется ещё одна фосфатная группа с высвобождением энергии и образованием АМФ (аденозин-монофосфата). АМФ гидролизу не подвергается.
Синтез АТФ
АТФ располагается в цитоплазме, ядре, хлоропластах, в митохондриях. Синтез АТФ в животной клетке происходит в митохондриях, а в растительной – в митохондриях и хлоропластах.
АТФ образуется из АДФ и фосфата с затратой энергии. Такой процесс называется фосфорилированием:
АДФ + Н3РО4 + энергия → АТФ + Н2О
Рис. 3. Образование АТФ из АДФ.
В растительных клетках фосфорилирование происходит при фотосинтезе и называется фотофосфорилированием. У животных процесс протекает при дыхании и называется окислительным фосфорилированием.
В животных клетках синтез АТФ происходит в процессе катаболизма (диссимиляции, энергетического обмена) при расщеплении белков, жиров, углеводов.
Функции
Из определения АТФ понятно, что эта молекула способна давать энергию. Помимо энергетической аденозинтрифосфорная кислота выполняет другие функции:
- является материалом для синтеза нуклеиновых кислот;
- является частью ферментов и регулирует химические процессы, ускоряя или замедляя их протекание;
- является медиатором – передаёт сигнал синапсам (местам контакта двух клеточных мембран).
Что мы узнали?
Из урока биологии 10 класса узнали о строении и функциях АТФ – аденозинтрифосфорной кислоты. АТФ состоит из аденина, рибозы и трёх остатков фосфорной кислоты. При гидролизе фосфатные связи разрушаются, что высвобождает энергию, необходимую для жизнедеятельности организмов.
Тест по теме
Оценка доклада
Средняя оценка: 4.6. Всего получено оценок: 106.
obrazovaka.ru
АТФ форма энергии в организме. Синтез АТФ. Цикл Кребса
Извлечение энергии из питательных веществ
text_fields
text_fields
arrow_upward
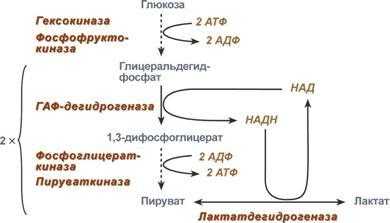
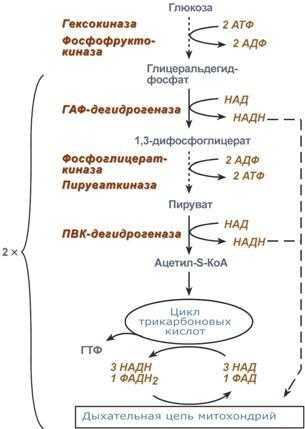
Извлечение энергии из питательных веществ — углеводов, белков, жиров происходит, в основном, внутри клетки. В ней все углеводы представлены глюкозой, белки — аминокислотами, жиры — жирными кислотами. В клетке глюкоза под влиянием энзимов цитоплазмы превращается в пировиноградную кислоту (в ходе анаэробного гликолиза) (рис. 1.6).
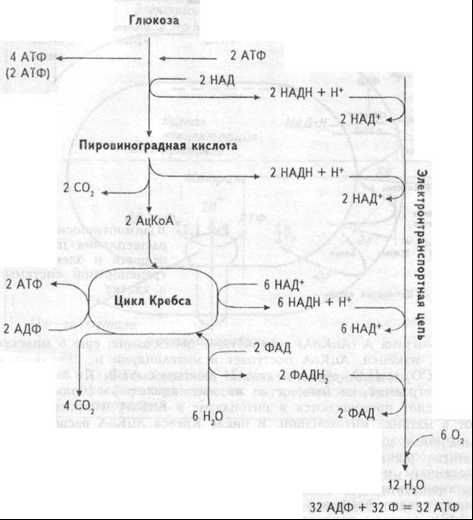 Рис. 1.6 Образование АТФ при полном окислении глюкозы
Рис. 1.6 Образование АТФ при полном окислении глюкозыВ ходе этих превращений из одной молекулы глюкозы образуется 2 молекулы АТФ (не считая 2 молекул АТФ, фосфорилирующих субстрат). Превращение пирувата в 2 молекулы ацетилкоэнзима А (АцКоА) способствует образованию еще 6 молекул АТФ. И, наконец, АцКоА поступает в митохондрии и, окисляясь в них до СО
| Источник энергии | Реакция | Выход молекул АТФ |
| Фосфолирирование субстрата | Гликолиз | 2 |
| 2 Н2 (4 Н) | Гликолиз | 4 |
| 2Н2(4 Н) | Пируват — АцКоА | 6 |
| Фосфорилирование субстрата | Цикл Кребса | 2 |
| 8Н2(16Н) | Цикл Кребса | 22 |
| 36АТФ |
В результате НАДН и НАДФН отдают один протон и два электрона в электротранспортную цепь, образуемую этими ферментами (рис.1.7).
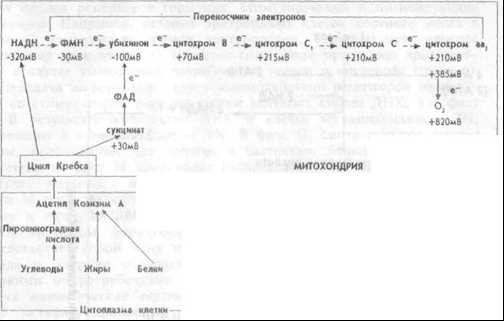 Рис.1.7 Взаимоотношения расщепления пищевых веществ и электрон-транспортной системы в клетке
Рис.1.7 Взаимоотношения расщепления пищевых веществ и электрон-транспортной системы в клеткеВ ходе передачи электронов в цепи переносчиков возрастают окислительно-восстановительные потенциалы — от отрицательных значений до потенциала восстановления О2. Эта разница окислительно-восстановительных потенциалов и образует ту движущую силу, которая приводит к синтезу АТФ. Описанный перенос электронов и протонов от НАДН и НАДФН по цепи транспорта электронов называется окислительным фосфорилированием. Согласно хемиосмотической теории, объясняющей механизм образования энергии при окислительном фосфорилировании, в ходе передачи электронов по электронно-транспортной цепи, пара электронов три раза пересекает внутреннюю мембрану митохондрий, каждый раз перенося два протона наружу (рис. 1.8).
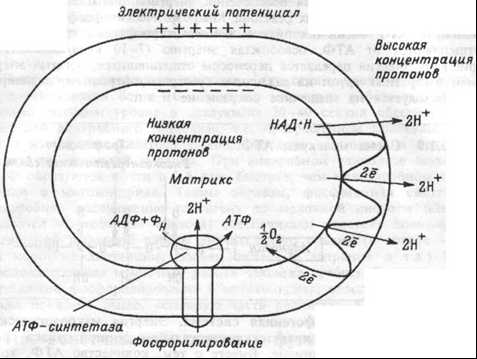 Рис. 1.8 Хемиосмотический механизм окислительного фосфорилирования во внутренней мембране митоходрий.
Рис. 1.8 Хемиосмотический механизм окислительного фосфорилирования во внутренней мембране митоходрий.В результате возникает высокая концентрация протонов снаружи мембраны, и низкая — в матриксе митохондрий и, как следствие, разница в электрическом потенциале между наружным (имеющим положительный заряд) и внутренним (накапливающим отрицательный заряд) слоем мембраны. Оба эти фактора (электрическое поле и разность концентраций) формируют электрохимический трансмембранный протонный градиент, благодаря которому протоны начинают возвращаться назад через мембрану. Это обратное движение протонов осуществляется через мембранный белок, к которому присоединяется АТФ-синтетаза, расположенная на внутренней (матричной) стороне мембраны. Взаимодействие мембранного белка с АТФ-синтетазой активирует ее и сопровождается синтезом АТФ из аденозин-дифосфорной (АДФ) и фосфорной кислот (Фн). Следовательно, поток протонов через мембрану активирует реакцию:
АДФ + Фн —> АТФ + Н2О
Энергия протонного градиента также обеспечивает транспорт ионов кальция и натрия через мембрану митохондрий, восстановление в них НАДФ+ с помощью НАДН, образование тепла. Молекулы АТФ, образовавшиеся в ходе гликолиза и окислительного фосфорилирования используются клеткой для обеспечения энергией почти всех внутриклеточных метаболических реакций.
Рис. 1.9 Схема молекулы АТФ. Стрелками показаны Тpuфocфam Высокоэнергетические связи.Макроэргические фосфатные связи молекулы АТФ очень нестойки и концевые фосфатные группы легко отщепляются от АТФ, освобождая энергию (7-10 ккал/моль АТФ) (рис. 1.9).
Энергия передается переносом отщепившихся, богатых энергией фосфатных групп на различные субстраты, ферменты, активируя их, расходуется на мышечное сокращение и т.п.
Энергетическая фосфогенная система
text_fields
text_fields
arrow_upward
Энергия макроэргических связей молекулы АТФ является универсальной формой запаса свободной энергии в организме. Вместе с тем, количество АТФ, хранимое внутри клетки невелико. Оно обеспечивает ее работу лишь в течение нескольких секунд. Это обстоятельство привело к формированию чувствительных механизмов, регулирующих энергетический обмен в скелетной, сердечной и нервных клетках. В этих тканях присутствуют органические фосфатные соединения, накапливающие энергию в форме фосфатных связей и представляющие собой источник этих богатых энергией фосфатных групп для синтеза АТФ. Органические фосфатные соединения получили название фосфагенов. Наиболее важным из них у человека является креатинфосфат (КФ). При его расщеплении высвобождается энергия до 10 ккал/моль, используемая для ресинтеза АТФ. Снижение содержания АТФ в этих тканях ведет к распаду КФ, а увеличение концентрации АТФ — к его ресинтезу. Так, в скелетной мышце концентрация КФ в 3-5 раз больше, чем АТФ. Гидролиз КФ (на креатин и фосфат) под влиянием фермента креатинкиназы обеспечивает ресинтез АТФ, являющейся источником энергии для мышечного сокращения:
Освободившийся креатин вновь используется клеткой для аккумуляции энергии в креатинфосфате. Этот эффект сохраняет концентрацию АТФ в клетке на относительно постоянном уровне. Поэтому фосфокреатин клеток скелетной мышцы и ее АТФ составляют, так называемую, энергетическую фосфогенную систему. Энергия фосфогенной системы используется для обеспечения «рывковой» мышечной активности, продолжительностью до 10-15 секунд, т.е. максимальной мышечной мощности, достаточной для бега на 100-метровую дистанцию.
Энергообеспечивающая система «гликоген-молочная кислота»
text_fields
text_fields
arrow_upward
Продолжающаяся более 10-15 секунд мышечная работа на максимально высоком уровне в следующие 30-40 секунд обеспечивается энергией анаэробного гликолиза, т.е. превращением молекулы глюкозы из расщепляющегося углеводного депо — гликогена печени и мышц до молочной кислоты. При анаэробном гликолизе молекулы АТФ образуются почти в 2,5 раза быстрее, чем при аэробном окислении в митохондриях. Таким образом, фосфогенная система и анаэробное расщепление гликогена до молочной кислоты (система гликоген — молочная кислота) обеспечивают человеку возможность мышечной рывковой работы значительного объема (в спорте — бег на короткие дистанции, подъем тяжестей, ныряние и т.д.) Более продолжительная мышечная работа человека требует усиления окислительного фосфорилирования в митохондриях, обеспечивающего, как было показано выше, основную часть ресинтеза АТФ.
doctor-v.ru
Строение и функции АТФ — Науколандия
В биологии аббревиатурой АТФ обозначают органическое вещество (мономер) аденозинтрифосфат (аденозинтрифосфорную кислоту). По химическому строению оно представляет собой нуклеозидтрифосфат. В состав АТФ входят рибоза, аденин, три остатка фосфорной кислоты. Фосфаты последовательно связаны между собой. При этом два последних так называемой макроэргической связью, разрыв которой обеспечивает клетку большим количеством энергии. Таким образом, АТФ выполняет в клетке энергетическую функцию.
Большая часть молекул АТФ образуется в митохондриях в реакциях клеточного дыхания. В клетках постоянно идет синтез и распад большого количество молекул аденозинтрифосфорной кислоты.
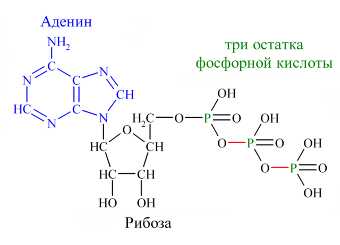 Химическое строение молекулы аденозинтрифосфата. Красным цветом обозначены макроэргические связи
Химическое строение молекулы аденозинтрифосфата. Красным цветом обозначены макроэргические связи
Отщепление фосфатных групп в основном происходит при участии фермента АТФ-азы и является реакцией гидролиза (присоединения воды):
АТФ + H2O = АДФ + H3PO4 + E,
где E — это выделяющаяся энергия, идущая на различные клеточные процессы (синтез других органических веществ, их транспорт, движение органоидов и клетки, терморегуляцию и др.). По разным источникам количество выделяющейся энергии составляет от 30 до 60 кДж/моль.
АДФ — это аденозиндифосфат, который содержит уже два остатка фосфорной кислоты. Чаще всего к нему потом снова присоединяется фосфат с образованием АТФ:
АДФ + H3PO4 = АТФ + H2O — E.
Эта реакция идет с поглощением энергии, накопление которой происходит в результате рада ферментативных реакций и процессов переноса ионов (в основном в матриксе и на внутренней мембране митохондрий). В конечном итоге энергия аккумулируется в присоединяемой к АДФ фосфатной группе.
Однако от АДФ может отщепиться еще один фосфат, связанный макроэргической связью, при это образуется АМФ (аденозинмонофосфата). АМФ входит в состав РНК. Отсюда еще одна функция аденозинтрифосфорной кислоты – она служит источником сырья для синтеза ряда органических соединений.
Таким образом, особенности строения АТФ, функциональное использование только его в качестве источника энергии в метаболических процессах, дает возможность клеткам иметь единую и универсальную систему по приему химической энергии.
Связанная статья: Этапы энергетического обмена
scienceland.info
Расчет атф при анаэробном окислении
На подготовительном этапе на активацию глюкозы затрачивается 2 молекулы АТФ, фосфат каждой из которых оказывается на триозе – глицеральдегидфосфате и диоксиацетонфосфате.
В следующий второй этап входят две молекулы глицеральдегидфосфата, каждая из которых окисляется до пирувата с образованием 2-х молекул АТФ в седьмой и десятой реакциях – реакциях субстратного фосфорилирования. Таким образом, суммируя, получаем, что на пути от глюкозы до пирувата в чистом виде образуется 2 молекулы АТФ.
Однако надо иметь в виду и пятую, глицеральдегидфосфат-дегидрогеназную, реакцию, из которой выходит НАДН. Если условия анаэробные, то он используется в лактатдегидрогеназной реакции, где окисляется для образования лактата и в получении АТФ не участвует.
|
Участки гликолиза, связанные с образованием и затратой энергии |
Расчет энергетического эффекта анаэробного окисления глюкозы |
Аэробное окисление
Если в клетке имеется кислород, то НАДН из гликолиза направляется в митохондрию (челночные системы), на процессы окислительного фосфорилирования, и там его окисление приносит дивиденды в виде трех молекул АТФ.
Образовавшийся в гликолизе пируват в аэробных условиях превращается в ПВК-‑дегидрогеназном комплексе(посмотреть) в ацетил-S-КоА, при этом образуется 1 молекула НАДН.
Ацетил-S-КоА вовлекается в ЦТК и, окисляясь, дает 3 молекулы НАДН, 1 молекулу ФАДН2, 1 молекулу ГТФ. Молекулы НАДН и ФАДН2 движутся в дыхательную цепь (посмотреть), где при их окислении в сумме образуется 11 молекул АТФ. В целом при сгорании одной ацетогруппы в ЦТК образуется 12 молекул АТФ.
Суммируя результаты окисления «гликолитического» и «пируватдегидрогеназного» НАДН, «гликолитический» АТФ, энергетический выход ЦТК и умножая все на 2, получаем 38 молекул АТФ.
|
Участки окисления глюкозы, связанные с образованием энергии |
Расчет энергетического эффекта аэробного окисления глюкозы |
Организм должен уметь синтезировать глюкозу
В клетках организма всегда существует потребность в глюкозе:
для эритроцитов глюкоза является единственным источником энергии,
нервная ткань потребляет около 120 г глюкозы в сутки и эта величина практически не зависит от интенсивности ее работы. Только в экстремальных ситуациях (длительное голодание) она способна получать энергию из неуглеводных источников,
глюкоза играет весомую роль для поддержания необходимых концентраций метаболитов цикла трикарбоновых кислот (в первую очередь оксалоацетата).
Таким образом, при определенных ситуациях – при низком содержании углеводов в пище, голодании, длительной физической работе, т.е. когда глюкоза крови расходуется и наступает гипогликемия, организм должен иметь возможность синтезировать глюкозу и нормализовать ее концентрацию в крови. Это достигается реакциями глюконеогенеза
По определению, глюконеогенез – это синтез глюкозы из неуглеводных компонентов: лактата, пирувата, глицерола, кетокислот цикла Кребса и других кетокислот, из аминокислот.
Необходимость глюконеогенеза в организме демонстрируют два цикла – глюкозо-лактатный и глюкозо-аланиновый.
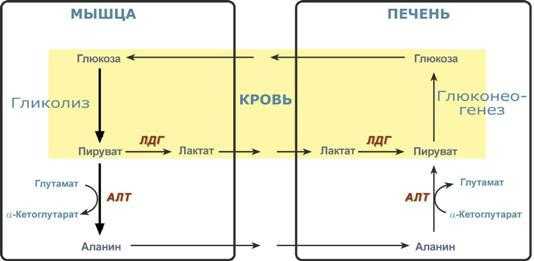
Глюкозо-лактатный цикл (цикл Кори)
Глюкозо-лактатный цикл – это циклический процесс, объединяющий реакции глюконеогенеза и реакции анаэробного гликолиза. Глюконеогенез происходит в печени, субстратом для синтеза глюкозы является лактат, поступающий в основном из эритроцитов или мышечной ткани.
В эритроцитах молочная кислота образуется непрерывно, так как для них анаэробный гликолиз является единственным способом образования энергии.
В скелетных мышцах высокое накопление молочной кислоты (лактата) является следствием гликолиза при очень интенсивной, субмаксимальной мощности, работе, при этом внутриклеточный рН снижается до 6,3-6,5. Но даже при работе низкой и средней интенсивности в скелетной мышце всегда образуется некоторое количество лактата.
Убрать молочную кислоту можно только одним способом – превратить ее в пировиноградную кислоту. Однако сама мышечная клетка ни при работе, ни во время отдыха не способна превратить лактат в пируват из-за особенностей изофермента лактатдегидрогеназы-‑5. Зато клеточная мембрана высоко проницаема для лактата и он движется по градиенту концентрации наружу. Поэтому во время и после нагрузки (при восстановлении) лактат легко удаляется из мышцы. Это происходит довольно быстро, всего через 0,5-‑1,5 часа в мышце лактата уже нет. Малая часть молочной кислоты выводится с мочой.
Большая часть лактата крови захватывается гепатоцитами, окисляется в пировиноградную кислоту и вступает на путь глюконеогенеза. Глюкоза, образованная в печени используется самим гепатоцитом или возвращается обратно в мышцы, восстанавливая во время отдыха запасы гликогена. Также она может распределиться по другим органам.
studfiles.net
Тема 3.2. Обмен веществ и превращение энергии. Энергетический обмен.
1. Дайте определения понятий.
Метаболизм – набор химических реакций, которые возникают в живом организме для поддержания жизни.
Энергетический обмен – процесс метаболического распада, разложения на более простые вещества или окисления какого-либо вещества, обычно протекающий с высвобождением энергии в виде тепла и в виде АТФ.
Пластический обмен – совокупность всех процессов биосинтеза, протекающих в живых организмах.
2. Заполните таблицу.
3. Изобразите схематично молекулу АТФ. Обозначьте ее части. Укажите расположение макроэргических связей. Напишите полное название этой молекулы.
АТФ – аденозинтрифосфорная кислота
4. К какому классу органических веществ относится АТФ? Почему вы сделали такой вывод?
Нуклеотид, так как состоит из аденина, рибозы и трех остатков фосфорной кислоты.
5. Пользуясь материалом § 3.2, заполните таблицу.
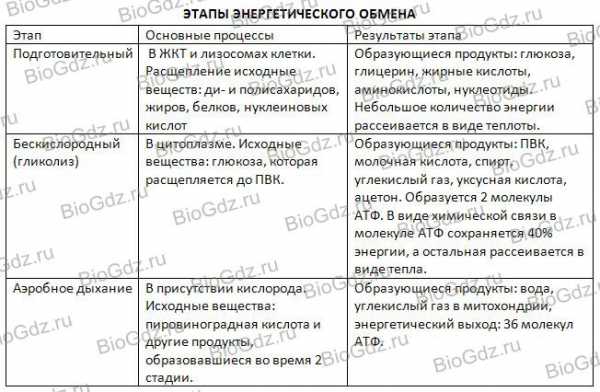
6. Какова биологическая роль ступенчатого характера энергетического обмена?
Постепенное выделение энергии, идущее в ходе энергетического обмена, позволяет более рационально использовать и запасать энергию. При разовом выделении такого числа энергии большая ее часть просто не успела бы соединиться с АДФ и выделилась бы как тепло, что означает большие потери для организма.
7. Объясните, почему кислород необходим большинству современных организмов. В результате какого процесса в клетках образуется углекислый газ?
Кислород необходим для дыхания. При наличии кислорода органические вещества при дыхании полностью окисляются до углекислого газа и воды.
8. Как повлияло накопление в атмосфере Земли кислорода на степень интенсивности процессов жизнедеятельности обитателей нашей планеты?
Кислород оказывает глубокое влияние на организм в целом, повышая общую энергию жизнедеятельности обитателей нашей планеты. Возникли и эволюционировали новые организмы.
9. Вставьте пропущенные слова.
Реакции пластического обмена идут с поглощением энергии.
Реакции энергетического обмена идут с выделением энергии.
Подготовительный этап энергетического обмена осуществляется в ЖКТ и лизосомах
клетки.
Гликолиз протекает в цитоплазме.
Во время подготовительного этапа белки под действием пищеварительных ферментов превращаются в аминокислоты.
10. Выберите правильный ответ.
Тест 1.
Какая из аббревиатур обозначает носителя энергии в живой клетке?
3) АТФ;
Тест 2.
На подготовительном этапе энергетического обмена белки распадаются до:
2) аминокислот;
Тест 3.
В результате бескислородного окисления в клетках животных при недостатке кислорода образуется:
3) молочная кислота;
Тест 4.
Энергия, которая выделяется в реакциях подготовительного этапа энергетического обмена:
2) рассеивается в виде тепла;
Тест 5.
Гликолиз обеспечивают ферменты:
3) цитоплазмы;
Тест 6.
При полном окислении четырех молекул глюкозы образуется:
4) 152 молекулы АТФ.
Тест 7.
Для наиболее быстрого восстановления работоспособности при усталости в период подготовки к экзамену лучше всего съесть:
3) кусок сахара;
11. Составьте синквейн к термину «метаболизм».
Метаболизм
Пластический и энергетический.
Синтезирует, разрушает, превращает.
Набор химических реакций в живом организме для поддержания жизни.
Обмен веществ.
12. Скорость обмена веществ непостоянна. Укажите некоторые внешние и внутренние причины, которые, по вашему мнению, способны изменять скорость обмена веществ.
Внешние – температура окружающей среды, физические нагрузки, масса тела.
Внутренние – уровень гормонов в крови, состояние нервной системы (угнетение или возбуждение).
13. Вы знаете, что существуют аэробные и анаэробные организмы. А кто такие факультативные анаэробы?
Это организмы, энергетические циклы которых проходят по анаэробному пути, но способные существовать при доступе кислорода, в отличие от облигатных анаэробов, для которых кислород губителен.
14. Объясните происхождение и общее значение слова (термина), опираясь на значение корней, его составляющих.
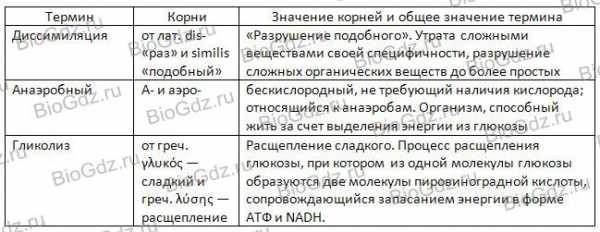
15. Выберите термин и объясните, насколько его современное значение соответствует первоначальному значению его корней.
Выбранный термин – гликолиз.
Соответствие: термин соответствует, но дополнен. Современное определение гликолиза, это не просто «расщепление сладкого», а процесс окисления глюкозы, при котором из одной ее молекулы образуются две молекулы ПВК, осуществляемый последовательно за несколько ферментативных реакций и сопровождающийся запасанием энергии в форме АТФ и NADH.
16. Сформулируйте и запишите основные идеи § 3.2.
Для любого организма характерен обмен веществ – набор хим. реакций для поддержания жизни. Энергетический обмен – процесс разложения на более простые вещества, протекающий с высвобождением энергии в виде тепла и в виде АТФ. Пластический обмен – совокупность всех процессов биосинтеза, протекающих в живых организмах.
Молекула АТФ – универсальный поставщик энергии в клетках.
Энергетический обмен протекает в 3 стадии: подготовительный этап (образуется глюкоза и тепло), гликолиз (образуется ПВК, 2 молекулы АТФ и тепло) и кислородный, или клеточное дыхание, (образуется 36 молекул АТФ и углекислый газ).
biogdz.ru
Дыхательная цепь: функциональные ферменты
Все биохимические реакции в клетках любого организма протекают с расходованием энергии. Дыхательная цепь – это последовательность специфических структур, которые расположены на внутренней мембране митохондрий и служат для образования АТФ. Аденозинтрифосфат является универсальным источником энергии и способен аккумулировать в себе от 80 до 120 кДж.
Дыхательная цепь электронов — что это такое?
Электроны и протоны играют важную роль в образовании энергии. Они создают разность потенциалов на противоположных сторонах мембраны митохондрий, что порождает направленное движение частиц – ток. Дыхательная цепь (она же ЭТЦ, цепь переноса электронов) является посредником при переносе положительно заряженных частиц в межмембранное пространство и отрицательно заряженных частиц в толще внутренней мембраны митохондрий.
Главная роль в образовании энергии принадлежит АТФ-синтазе. Этот сложный комплекс видоизменяет энергию направленного движения протонов в энергию биохимических связей. К слову, практически идентичный комплекс находится и в хлоропластах растений.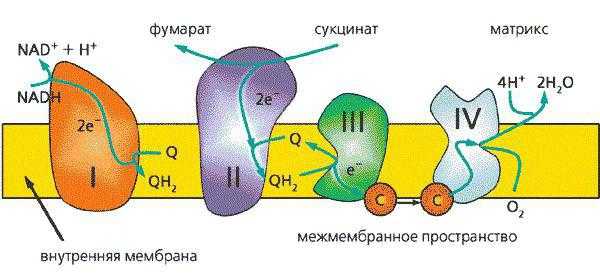
Комплексы и ферменты дыхательной цепи
Перенос электронов сопровождается биохимическими реакциями в присутствии ферментативного аппарата. Эти биологически активные вещества, многочисленные копии которых образуют большие комплексные структуры, служат посредниками при переносе электронов.
Комплексы дыхательной цепи – это центральные компоненты транспортировки заряженных частиц. Всего во внутренней мембране митохондрий находятся 4 таких образования, а также АТФ-синтаза. Все эти структуры объединены общей целью – перенос электронов по ЭТЦ, перенос протонов водорода в межмембранное пространство и, как следствие, синтез АТФ.
Комплекс представляет собой скопление белковых молекул, среди которых встречаются ферменты, структурные и сигнальные протеины. Каждый из 4 комплексов выполняет свою, только свойственную ему, функцию. Давайте разберемся, для каких задач в ЭТЦ присутствуют эти структуры.
I комплекс
В переносе электронов в толще мембраны митохондрий главную роль выполняет дыхательная цепь. Реакции отщепления протонов водорода и сопутствующих им электронов – одна из центральных реакций ЭТЦ. Первый комплекс транспортной цепи принимает на себя молекулы НАД*Н+ (у животных) или НАДФ*Н+ (у растений) с последующим отщеплением четырех протонов водорода. Собственно, из-за этой биохимической реакции I комплекс также называется НАДН – дегидрогеназой (по названию центрального фермента).
В состав дегидрогеназного комплекса входят железосерные белки 3 видов, а также флавинмононуклеотиды (ФМН).
II комплекс
Работа данного комплекса не сопряжена с переносом протонов водорода в межмембранное пространство. Основная функция этой структуры заключается в поставке дополнительных электронов в электрон-транспортную цепь посредством окисления сукцината. Центральный фермент комплекса – сукцинат-убихинон-оксидоредуктаза, который катализирует отщепление электронов от янтарной кислоты и перенос на липофильный убихинон.
Поставщиком протонов водорода и электронов ко второму комплексу также является ФАД*Н2. Однако КПД флавинадениндинуклеотида меньше, чем у его аналогов – НАД* Н или НАДФ*Н.
В состав II комплекса входят три вида железосерных белков и центральный фермент сукцинат-оксидоредуктаза.
III комплекс
Следующий по счету компонент, ЭТЦ, состоит из цитохромов b556,b560 и c1, а также железосерного белка Риске. Работа третьего комплекса сопряжена с переносом двух протонов водорода в межмембранное пространство, и электронов от липофильного убихинона на цитохром С.
Особенностью белка Риске является то, что он растворяется в жире. Другие протеины этой группы, которые встречались в составе комплексов дыхательной цепи, водорастворимы. Эта особенность влияет на положение белковых молекул в толще внутренней мембраны митохондрий.
Третий комплекс функционирует как убихинон-цитохром с-оксидоредуктаза.
IV комплекс
Он же цитохром-оксидантный комплекс, является конечным пунктом в ЭТЦ. Его работа заключается в переносе электрона с цитохрома-с на атомы кислорода. Впоследствии отрицательно заряженные атомы О будут вступать в реакцию с протонами водорода с образованием воды. Главный фермент – цитохром с-кислород-оксидоредуктаза.
В состав четвертого комплекса входят цитохромы a, a3 и два атома меди. Центральная роль в переносе электрона к кислороду досталась цитохрому a3. Взаимодействие этих структур подавляется цианидом азота и угарным газом, что в глобальном смысле приводит к прекращению синтеза АТФ и гибели.
Убихинон
Убихинон – это витаминоподобное вещество, липофильное соединение, которое свободно перемещается в толще мембраны. Дыхательная цепь митохондрий не может обойтись без этой структуры, т. к. она отвечает за транспортировку электронов от комплексов I и II к комплексу III.
Убихинон является производным бензохинона. Эта структура на схемах может обозначаться буквой Q или сокращенно ЛУ (липофильный убихинон). Окисление молекулы приводит к образованию семихинона – сильного окислителя, который потенциально опасен для клетки.
АТФ-синтаза
Главная роль в образовании энергии принадлежит АТФ-синтазе. Эта грибоподобная структура использует энергию направленного движения частиц (протонов) для преобразования ее в энергию химических связей.
Основной процесс, который встречается на протяжении всей ЭТЦ, — это окисление. Дыхательная цепь отвечает за перенос электронов в толще мембраны митохондрий и аккумулирование их в матриксе. Одновременно с этим комплексы I, III и IV перекачивают протоны водорода в межмембранное пространство. Разница зарядов на сторонах мембраны приводит к направленному движению протонов через АТФ-синтазу. Так Н+ попадают в матрикс, встречают электроны (которые связаны с кислородом) и образуют нейтральное для клетки вещество – воду.
АТФ-синтаза состоит из F0и F1 субъединиц, которые вместе образуют роутер молекулы. F1 состоит из трех альфа и трех бета-субъединиц, которые вместе образуют канал. Этот канал имеет в точности такой же диаметр, какой имеют протоны водорода. При прохождении положительно заряженных частиц через АТФ-синтазу головка F0 молекулы крутится на 360 градусов вокруг своей оси. За это время к АМФ или АДФ (аденозинмоно- и дифосфат) присоединяются фосфорные остатки с помощью макроэргических связей, в которых заключено большое количество энергии.
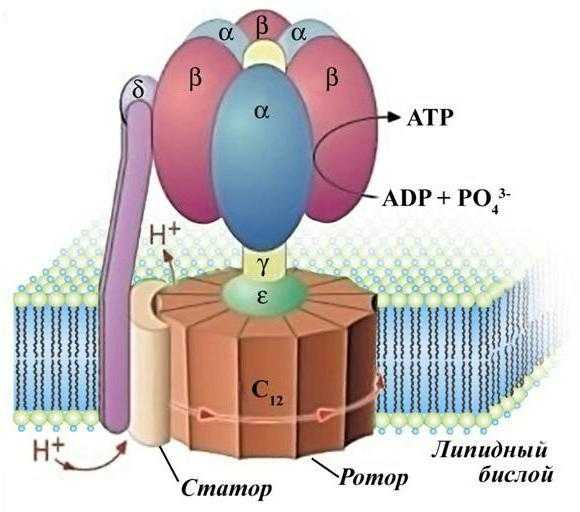
АТФ-синтазы встречаются в организме не только в митохондриях. У растений эти комплексы также расположены на мембране вакуолей (тонопласте), а также на тилакоидах хлоропласт.
Также в клетках животных и растений присутствуют АТФ-азы. Они имеют схожую структуру, как и у АТФ-синтаз, однако их действие направлено на отщепление фосфорных остатков с затратой энергии.
Биологический смысл дыхательной цепи
Во-первых, конечным продуктом реакций ЭТЦ является так называемая метаболическая вода (300-400 мл в сутки). Во-вторых, происходит синтез АТФ и запасание энергии в биохимических связях этой молекулы. В сутки синтезируется 40-60 кг аденозинтрифосфата и столько же используется в ферментативных реакциях клетки. Срок жизни одной молекулы АТФ составляет 1 минуту, поэтому дыхательная цепь должна работать слаженно, четко и без ошибок. В противном случае клетка погибнет.
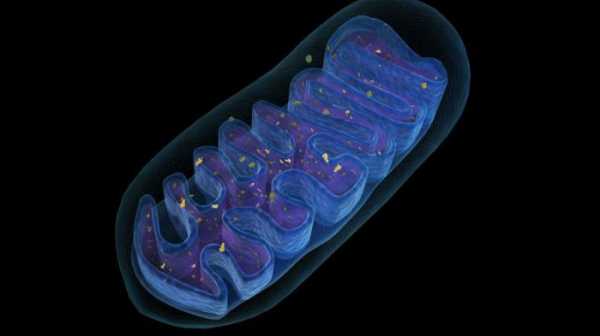
Митохондрии считаются энергетическими станциями любой клетки. Их количество зависит от энергозатрат, которые необходимы для тех или иных функций. Например, в нейронах можно насчитать до 1000 митохондрий, которые часто образуют скопление в так называемой синаптической бляшке.
Отличия дыхательной цепи у растений и животных
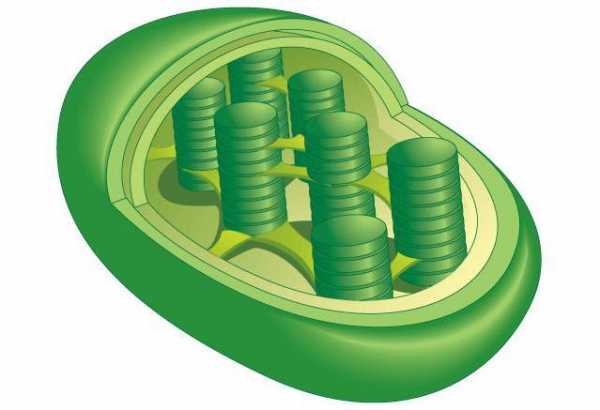
У растений дополнительной «энергетической станцией» клетки является хлоропласт. На внутренней мембране этих органелл также найдены АТФ-синтазы, и это является преимуществом перед животными клетками.
Также растения могут выживать в условиях высокой концентрации угарного газа, азота и цианидов за счет цианид-устойчивого пути в ЭТЦ. Дыхательная цепь, таким образом, заканчивается на убихиноне, электроны с которого сразу переносятся на атомы кислорода. В результате синтезируется меньше АТФ, однако растение может пережить неблагоприятные условия. Животные в таких случаях при длительном воздействии погибают.
Можно сравнить КПД НАД, ФАД и цианид-устойчивого пути с помощью показателя образования АТФ при переносе 1 электрона.
- с НАД или НАДФ образуется 3 молекулы АТФ;
- с ФАД образуется 2 молекулы АТФ;
- по цианид-устойчивому пути образуется 1 молекула АТФ.

Эволюционное значение ЭТЦ
Для всех эукариотических организмов одним из основных источников энергии является дыхательная цепь. Биохимия синтеза АТФ в клетке делится на два типа: субстратное фосфорилирование и окислительное фосфорилирование. ЭТЦ используется в синтезе энергии второго типа, т. е. за счет окислительно-восстановительных реакций.
У прокариотических организмов АТФ образуется только в процессе субстратного фосфорилирования на стадии гликолиза. Шестиуглеродные сахара (преимущественно глюкоза) вовлекаются в цикл реакций, и на выходе клетка получает 2 молекулы АТФ. Этот тип синтеза энергии считается наиболее примитивным, т. к. у эукариот в процессе окислительного фосфорилирования образуется 36 молекул АТФ.
Однако это не значит, что современные растения и животные потеряли способность к субстратному фосфорилированию. Просто этот тип синтеза АТФ стал только одним из трех этапов получения энергии в клетке.
Гликолиз у эукариот проходит в цитоплазме клетки. Там находятся все необходимые ферменты, которые смогут расщепить глюкозу до двух молекул пировиноградной кислоты с образованием 2 молекул АТФ. Все последующие этапы проходят в матриксе митохондрий. Цикл Кребса, или цикл трикарбоновых кислот, также протекает в митохондриях. Это замкнутая цепь реакций, в результате работы которой синтезируются НАД*Н и ФАД*Н2. Эти молекулы пойдут как расходный материал в ЭТЦ.
fb.ru
ЛЕКЦИЯ Структурная организация дыхательной цепи
Биологическое окисление – совокупность реакций окисления субстратов в живых клетках, основная функция которых – энергетическое обеспечение метаболизма.
Главные функции окислительных процессов:
1) запас энергии в утилизируемой форме,
2) рассеяние энергии в виде теплоты,
3) образование полезных соединений,
4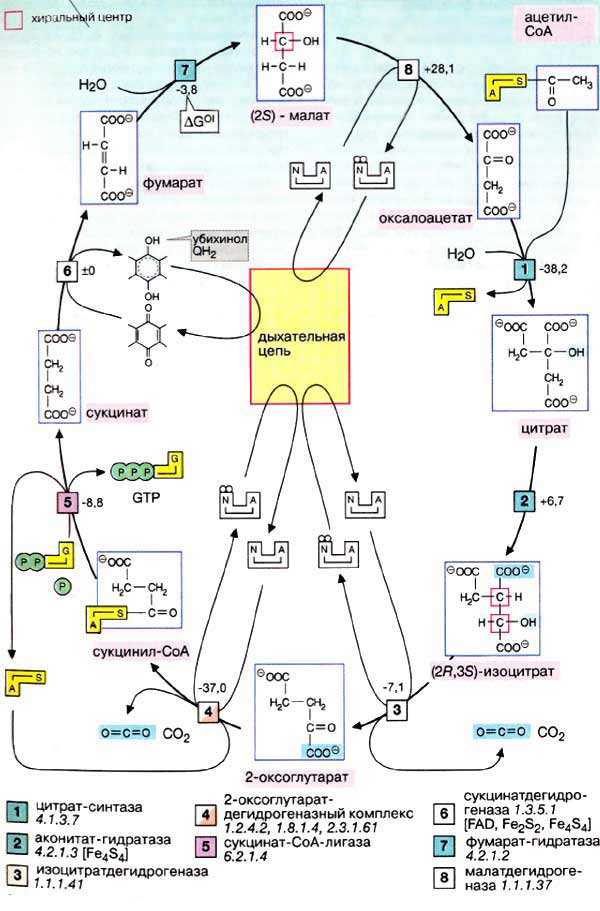 )
расщепление вредных веществ.
)
расщепление вредных веществ.
Различия между биологическим окислением и горением
Биологическое окисление не является одноступенчатой экзотермической реакцией, а представляет цепь реакций, в течение которых энергия освобождается, рассеивается в виде тепла и аккумулируется в АТФ.
При сгорании органических веществ освобождение энергии происходит за счёт окисления углерода до углекислого газа, а при биологическом окислении за счёт окисления водорода, восстановления кислорода до воды.
История развития учения о биологическое окислении.
Оксидазная теория А. Н. Баха
а) оксигеназа + О2 оксигеназа + перекись
б) оксигеназа + субстрат оксигеназа + окисленный субстрат.
Теория В. И. Палладина
Сущность окисления
Химические реакции, в процессе которых происходит перенос электрона от одной молекулы к другой, называются окислительно-восстановительными.
Соединения, отдающие электрон, доноры электрона или восстановители.
акцепторы электрона или окислители.
Fe + ē Fe
окислитель, восстановитель,
акцептор донор
Каждая редокс-пара характеризуется стандартным потенциалом ( в вольтах)
Редокс-потенциал
При сравнении редокс-потенциала системы с нормальным водородным электродом, потенциал которого равен нулю, получают величины, отражающие окислительно-восстановительные способности вещества.
Тканевое дыхание – вид биологического окисления, при котором акцептором электрона является кислород
Субстраты тканевого дыхания:
кислоты цикла Кребса (изоцитрат, а-кетоглутарат, сукцинат, малат),
ПВК,
лактат,
аминокислоты,
α-глицерофосфат,
жирные кислоты.
Осуществляется тканевое дыхание с помощью ферментов дыхательной цепи.
Схема превращения энергии в живых клетках: тканевое дыхание, образование АТФ и пути его использования.
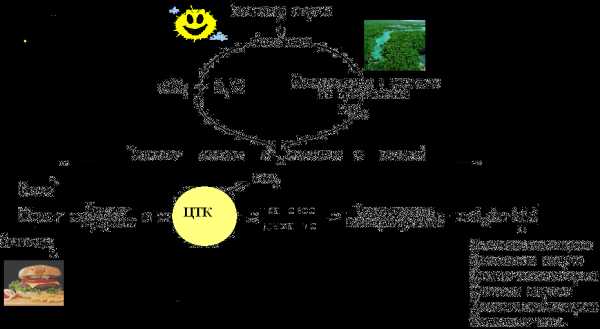
С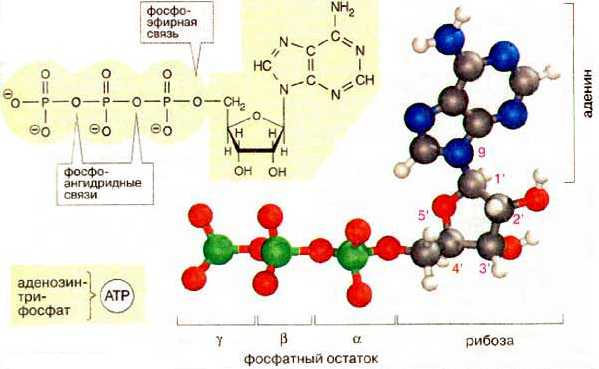 труктура
АТФ
труктура
АТФ
Способы синтеза АТФ
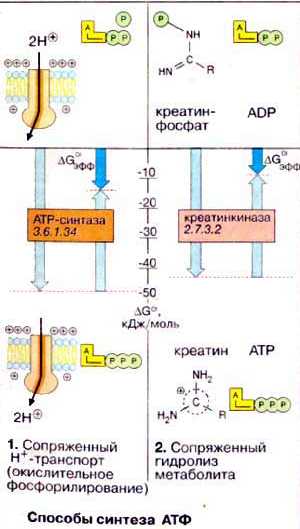
Дыхательная цепь – последовательность оксидоредуктаз во внутренней мембране митохондрий, осуществляющих перенос электронов и протонов от субстрата на молекулярный кислород.
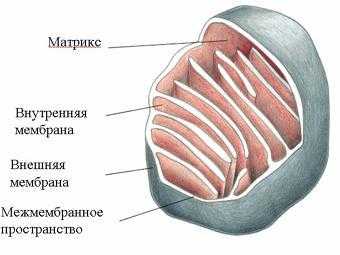
Митохондрия
Перенос электронов и протонов с участием промежуточных переносчиков.
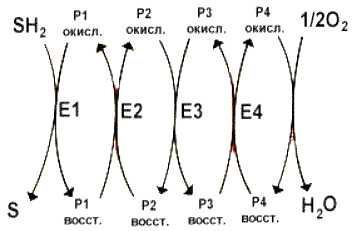
Sh3 — исходный донор протонов и электронов;
P1, Р2, Р3, Р4 — промежуточные переносчики;
E1, E2, E3, E4 — ферменты окислительно-восстановительных реакций
Компоненты дыхательной цепи
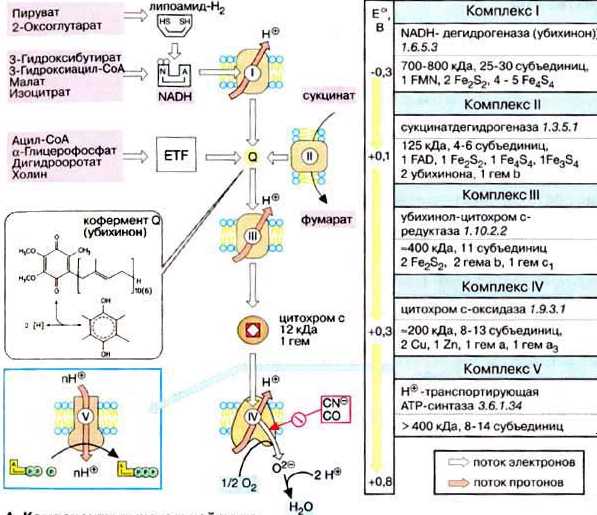
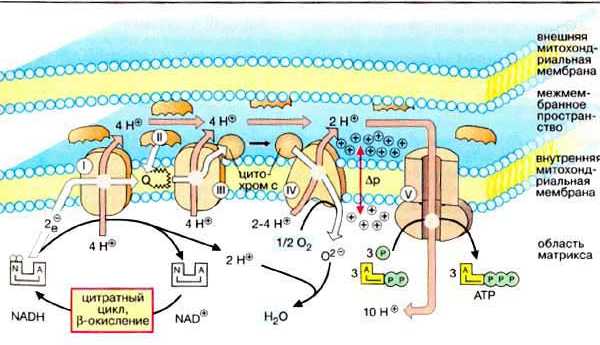
Водород в дыхательную цепь постыпает в виде в виде НАДН2, так как большинство дегидрогеназ внутри митохондрий НАД-зависимые, а также при действии на субстратфлавиновой дегидрогеназы (кофермент ФАД).
НАД-зависимые дегидрогеназы
S -HH +НАД+ S +НАДН+Н+
Цитозольный и митохондриальный пулы НАД и НАДФ отделены друг от друга митохондриальной мембраной, которая для этих коферментов непроницаема.
Челночные механизмы переносят восстановленные нуклеотиды (НАДН+Н ) из цитоплазмы в митохондрии/
В митохондриях под действием митохондриальной МДГ малат переходит в ЩУК, а НАДН+Н передаёт электроны и протоны в дыхательную цепь.
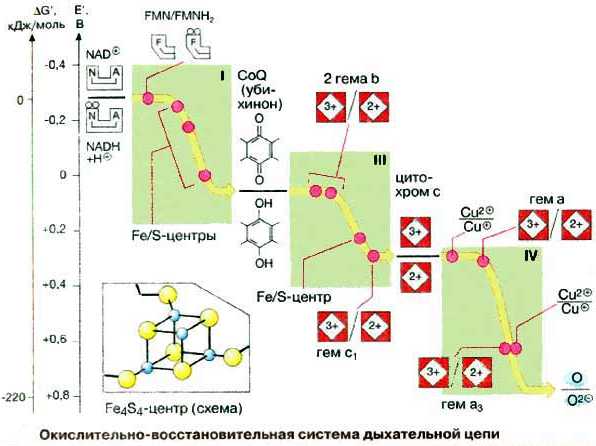
Окислительно-восстано-вительная система дыхательной цепи
Д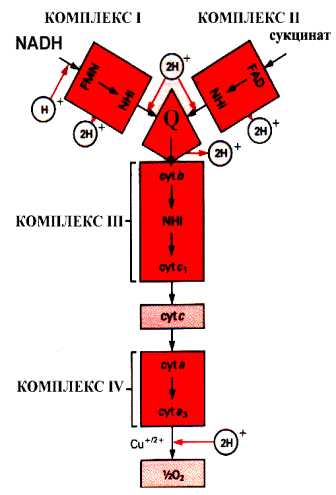 ыхательная
цепь включает 4 ферментных комплекса,
катализирующих окисление НАДН+Н
кислородом.
ыхательная
цепь включает 4 ферментных комплекса,
катализирующих окисление НАДН+Н
кислородом.
НАДН-KoQ-редуктаза катализирует перенос электронов от НАДН к KoQ.
Этот комплекс включает в себя:
НАДН-дегидрогеназа
ФМН + НАДН+Н ФМНН2 +НАД
В FeS – белках железо связано с остатком серы.
Сукцинат-KoQ-редуктаза катализирует перенос электронов от сукцината к KoQ
Этот комплекс включает в себя:
СДГ- флавопротеин,
прочно связан с внутренней мембраной митохондрий.
Коферментом является ФАД.
KoQ (убихинон)
KoQ + ФМНН2 KoQН2 + ФМН
Убихинон – коллектор, так как собирает восстановленные
эквиваленты не только от НАДН-ДГ, но и от СДГ
и других компонентов.
KoQН2 – цитохром С–редуктаза катализирует перенос электронов от KoQН2 к цитохрому
Комплекс включает в себя:
Цитохромы – сложные железосодержащие белки, окрашенные в красный цвет.
Кофермент аналогичен гему, но железо в цитохромах меняет валентность.
Впервые описаны Мак-Мунном, изучены Кейлиным.
Цитохромы переносят электроны.
Известны 25-30 различных цитохромов, которые отличаются:
спектром поглощения,
молекулярным весом,
растворимостью в воде.
П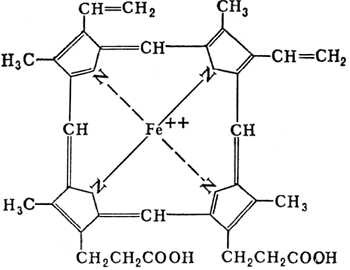 ростетическая
группа гема в структуре цитохромов.
ростетическая
группа гема в структуре цитохромов.
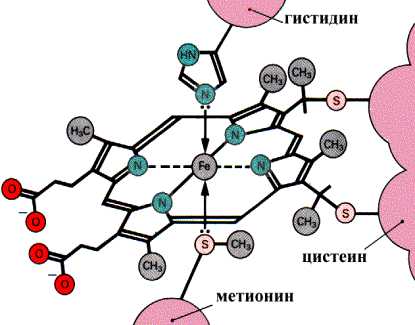
Связывание гема с белковой частью цитохрома С
Цитохромоксидаза катализирует перенос электронов от цитохрома С к кислороду.
Комплекс включает в себя:
цитохром а,
цитохром а3,
негемовое Fe,
липиды,
белки.
Цитохромоксидаза отличается от других цитохромов:
наличие меди,
реагирует с кислородом,
протонный насос.
В этом ферменте 4 редокс-центра:
Цитохром С СuА гем А гем а3 СuВ О2
Сu + е Сu
При транспорте одного электрона происходит перенос двух ионов водорода, один из которых используется при восстановлении кислорода до воды, а другой пересекает мембрану.
Кислород, поступающий в митохондрии из крови, связывается с атомом железа в геме цитохрома а.
Затем каждый из атомов молекулы кислорода
присоединяет по 2 электрона и по 2 протона,
превращаясь в молекулу воды.
Протоны поступают из водной среды.
4ē + 4Н + О2 2Н20
200 – 400 мл воды синтезируется в сутки – эндогенная вода.
Весь процесс окисления НАДН+Н в дыхательной цепи сопряжён с переносом 10Н с внутренней стороны мембраны наружу.
В этом процессе участвуют комплексы I, III, IV.
Комплекс II переносит водород от сукцината к KoQ. Этот комплекс не принимает непосредственного участия в образовании энергии.
Нарушения в работе дыхательной цепи
Состояние фатальной детской митохондриальной миопатии и дисфункции почек.
Связано со снижением активности или полным отсутствием большинства оксидоредуктаз дыхательной цепи.
Порядок распределения ферментов в дыхательной цепи определяется редокс-потенциалом.
Редокс-потенциал изменяется в цепи, так как электроны теряют свободную энергию, проходя по цепи, переходят на более низкий энергетический уровень.
Субстрат должен иметь более отрицательный потенциал, чем переносчик-фермент:
Глюкоза (-0,5 В) включается в самом начале дыхательной цепи.
Аскорбиновая кислота (+ 0,2 В) включается с цитохрома С1.
Электроны могут пройти через все переносчики от субстрата к кислороду.
Укороченные цепи
Сукцинат отдаёт электроны на ФАД КоQ цитохромы О2. Редокс-потенциал сукцината -0,13.
Аминокислоты флавиновые ферменты (оксидазы аминокислот) О2 Н2О2.
Ингибиторы дыхания
Инсектицид ротенон блокирует НАДН-ДГ. Барбитураты блокируют переход от ФП к убихинону.
Антимицин А блокирует стадию: цитохром В цитохром С.
Цианиды, угарный газ – ингибиторы цитохромоксидазы. Синильная кислота реагирует с Fe, угарный газ с Fe.
Каскадное выделение энергии в дыхательной цепи
Прохождение электрона по цепи сопровождается ступенчатым, этапным, дробным выделением энергии.
Общий перепад энергии в дыхательной цепи от – 0,32 до +0,82 составляет 1,14 В.
Выделенная каскадно энергия может быть утилизирована.
Перенос одной пары электронов от НАДН+Н к кислороду даёт 52,6 ккал.
Поскольку энергия электронов не может «откладываться про запас», она превращается в энергию химических связей АТФ.
Различают 2 типа дыхательных цепей:
сопряжённые с транспортом энергии,
несопряжённые с транспортом энергии.
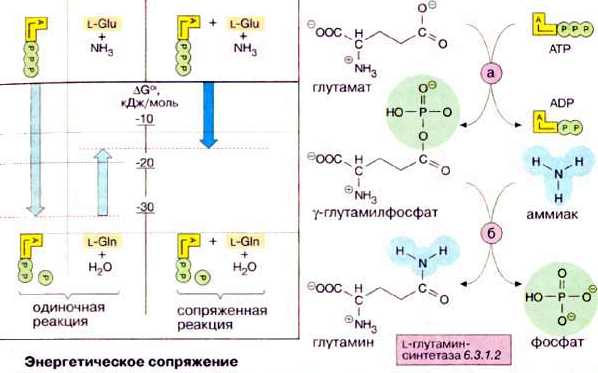
Тканевое дыхание включает:
отнятие водорода от субстрата,
многоэтапный процесс переноса электронов на кислород.
Перенос электронов сопровождается уменьшением свободной энергии.
Часть энергии рассеивается в виде тепла, а 40% используется на синтез АТФ.
studfiles.net